Resumen
1. Introducción
La hiperplasia benigna de próstata (HBP) es una de las enfermedades urológicas más prevalentes en hombres de edad avanzada, con evidencia histológica presente en hasta el 80–90% de los hombres en su séptima y octava décadas de vida [1]. Los inhibidores de la 5-alfa reductasa (5-ARI) finasterida y dutasterida representan un pilar del tratamiento médico de la HBP, actuando mediante el bloqueo de la conversión intraprostática de testosterona en dihidrotestosterona (DHT), el andrógeno principal responsable del crecimiento y desarrollo prostático [2][3].
Si bien los 5-ARI son reconocidos principalmente por su capacidad de reducir el volumen prostático en un 20–30% y disminuir el riesgo de retención aguda de orina y cirugía relacionada con HBP [4][5], un efecto cada vez mejor caracterizado pero infraestimado es su capacidad para reducir la vascularización prostática. Esta propiedad antiangiogénica tiene relevancia clínica directa: un metaanálisis reciente de 30 ensayos clínicos aleatorizados por Hehir et al. (2026) demostró que la administración preoperatoria de 5-ARI reduce significativamente la pérdida sanguínea intraoperatoria (diferencia media −82,58 mL), la caída de hemoglobina (−0,90 g/dL), las tasas de transfusión (OR 0,31) y el tiempo operatorio durante la RTUp [6].
El objetivo de esta revisión es delinear los mecanismos moleculares y celulares a través de los cuales los 5-ARI logran la regresión vascular prostática, y discutir las implicaciones traslacionales para la práctica quirúrgica, incluyendo su potencial relevancia para las técnicas modernas de enucleación.
2. El eje DHT–VEGF: el mecanismo central
El mecanismo principal a través del cual los 5-ARI reducen la vascularización prostática es la disrupción de la vía de señalización del VEGF dependiente de andrógenos. En condiciones fisiológicas e hiperplásicas, la DHT actúa como un potente estimulador de la expresión de VEGF en las células estromales y epiteliales prostáticas [7][8]. El VEGF, a su vez, es el factor proangiogénico dominante responsable de impulsar la neovascularización dentro de la próstata hiperplásica [9].
La concentración intraprostática de DHT es aproximadamente cinco veces mayor que la de testosterona, debido a la actividad de la 5-alfa reductasa [10][11]. La finasterida, que inhibe selectivamente la isoenzima tipo 2, reduce la DHT sérica en aproximadamente un 70%, mientras que la dutasterida, inhibidor dual de los tipos 1 y 2, alcanza una supresión superior al 90–95% [12][13]. Esta reducción de DHT intraprostática conduce a una regulación a la baja significativa de la expresión de VEGF en el tejido prostático.
Pareek et al. (2003) demostraron que los pacientes tratados con finasterida sometidos a RTUp presentaban una expresión de VEGF y una densidad microvascular (DMV) significativamente menores en el tejido prostático suburetral en comparación con los controles no tratados (p < 0,05) [14]. Es importante destacar que la reducción del VEGF fue más pronunciada en el compartimento suburetral, precisamente el tejido más relevante para el sangrado perioperatorio durante los procedimientos transuretrales.
Häggström et al. (1999) habían demostrado previamente en un modelo de castración que la testosterona induce directamente la síntesis de VEGF en la próstata ventral de rata, estableciendo el vínculo mecanístico entre la señalización androgénica y la angiogénesis prostática [15]. Los 5-ARI replican este efecto farmacológicamente al reducir la DHT sin deprivación androgénica completa.
3. Reducción de la densidad microvascular: evidencia en estudios humanos
Múltiples estudios clínicos han confirmado que el tratamiento con 5-ARI reduce la DMV en el tejido prostático humano. Hochberg et al. (2002) fueron los primeros en reportar una disminución significativa de la DMV suburetral en próstatas tratadas con finasterida mediante inmunohistoquímica con CD34 [16]. Este hallazgo fue posteriormente confirmado por Memis et al. (2008), quienes demostraron una reducción de la DMV específicamente en la zona suburetral tras 4 semanas de terapia con finasterida [17].
Un hallazgo crítico de Donohue et al. (2005) fue que incluso un curso corto de finasterida de 2 semanas puede reducir significativamente la DMV prostática y la expresión de VEGF en un entorno aleatorizado y controlado con placebo. En 64 pacientes aleatorizados a finasterida 5 mg o placebo antes de RTUp, la DMV fue 60 vs 71 y las puntuaciones de VEGF fueron 47 vs 61 (p < 0,01 y p < 0,001, respectivamente) [18b]. Este efecto rápido — que precede a la reducción volumétrica significativa de la glándula — indica que el mecanismo antiangiogénico de los 5-ARI es independiente de sus propiedades de reducción glandular y representa un efecto farmacológico primario.
El metaanálisis de Hehir et al. agrupó datos de múltiples ECAs y confirmó una reducción significativa de la DMV (DM = −6,18 vasos/mm³, p < 0,001) y de la expresión de VEGF (DM = −3,25, p < 0,001) en las muestras tratadas con 5-ARI, proporcionando evidencia de nivel 1 para este efecto [6].
4. Apoptosis de células endoteliales y regresión vascular
Más allá de la supresión de la señalización proangiogénica, los 5-ARI promueven activamente la regresión de la microvasculatura prostática existente a través de la inducción de apoptosis. Sutton et al. (2006) demostraron que el tratamiento con finasterida produce un aumento significativo del índice apoptótico (mediante ensayo TUNEL) y una reducción de la DMV (tinción con Factor VIII) en muestras prostáticas de pacientes con HBP tratados durante 1–12 meses en comparación con controles no tratados (p < 0,01) [19].
El mismo estudio demostró que la finasterida inhibe la adhesión celular del epitelio prostático in vitro, sugiriendo un mecanismo adicional por el cual el fármaco altera la integridad estructural del tejido prostático y su red de soporte vascular. Los autores propusieron que la finasterida actúa sobre la vascularización prostática mediante un doble mecanismo: induciendo apoptosis tanto en el compartimento endotelial como epitelial, e inhibiendo las interacciones de adhesión célula-célula necesarias para el mantenimiento vascular [19].
Rittmaster et al. (1995) proporcionaron evidencia previa de apoptosis y atrofia inducidas por finasterida en la próstata ventral de rata, demostrando que el tratamiento con 5-ARI conduce a atrofia ductal a través de muerte celular programada en lugar de simple quiescencia [20]. Este proceso apoptótico en los compartimentos epitelial y estromal reduce la demanda metabólica del tejido prostático, disminuyendo aún más la señalización paracrina que sostiene la red microvascular.
5. Modulación de HIF-1α y mediadores angiogénicos adicionales
Lekas et al. (2006) evaluaron los efectos de la finasterida sobre el factor inducible por hipoxia-1α (HIF-1α), VEGF y DMV en tejido prostático resecado de pacientes con HBP. Encontraron reducciones estadísticamente significativas en los tres parámetros en las muestras tratadas con finasterida en comparación con los controles [21]. HIF-1α es un factor de transcripción maestro que responde a la hipoxia tisular regulando al alza un conjunto de genes proangiogénicos, incluyendo VEGF, factor de crecimiento de fibroblastos (FGF) y factor de crecimiento derivado de plaquetas (PDGF) [22].
La reducción de HIF-1α por finasterida sugiere que los 5-ARI pueden interrumpir un programa angiogénico más amplio impulsado por la hipoxia en la próstata hiperplásica, en lugar de actuar únicamente a través de la supresión de VEGF. En el tejido prostático hiperplásico, el adenoma en expansión crea áreas de hipoxia relativa que estimulan la neovascularización mediada por HIF-1α. Al reducir simultáneamente tanto la masa tisular (y por tanto la demanda hipóxica) como la vía directa androgénica del VEGF, los 5-ARI logran un efecto antiangiogénico sinérgico.
Ku et al. (2009) extendieron estos hallazgos a dutasterida, demostrando reducciones similares en la expresión de HIF-1α y VEGF tanto en tejido prostático de rata como humano, apoyando un efecto de clase más que un fenómeno específico de finasterida [23].
Tabla 1
| Estudio / Año | Diseño | Tratamiento | Duración | N | Principales hallazgos | Compartimento | p-valor clave | Ref |
|---|---|---|---|---|---|---|---|---|
| Pareek et al. 2003 | Observacional comparativo | Finasterida 5 mg | Variable (pre-RTUp) | ~24 | ↓ Expresión de VEGF y ↓ DMV suburetral (CD34) | Suburetral | p < 0,05 | [14] |
| Hochberg et al. 2002 | Comparativo | Finasterida | Variable | ~20–30 | ↓ DMV suburetral (CD34) en pacientes con hematuria/HBP | Suburetral | Significativo | [16] |
| Memis et al. 2008 | Prospectivo comparativo | Finasterida 5 mg | 4 semanas | 30 | ↓ DMV suburetral significativa vs controles | Suburetral | Significativo | [17] |
| Donohue et al. 2005 | ECA controlado con placebo | Finasterida 5 mg | 2 semanas | 64 | ↓ DMV (60 vs 71) y ↓ VEGF (47 vs 61) en tejido post-RTUp | Prostático (post-RTUp) | DMV p < 0,01; VEGF p < 0,001 | [18b] |
| Lekas et al. 2006 | Comparativo | Finasterida | Variable | No espec. | ↓ HIF-1α, ↓ VEGF, ↓ DMV en tejido resecado | Prostático | Significativo | [21] |
| Sutton et al. 2006 | Comparativo + in vitro | Finasterida | 1–12 meses | 27 | ↑ Índice apoptótico (TUNEL), ↓ DMV (Factor VIII), ↓ adhesión celular | Prostático | p < 0,01 | [19] |
| Ku et al. 2009 | Comparativo (rata + humano) | Dutasterida | Variable | N/A (modelo mixto) | ↓ HIF-1α y ↓ VEGF en tejido prostático humano y de rata | Prostático | Significativo | [23] |
| Hehir et al. 2026 | Metaanálisis (30 ECAs) | 5-ARI (fin/dut) | Variable (incl. 2 sem.) | 2974 | ↓ DMV (DM −6,18 vasos/mm³); ↓ VEGF (DM −3,25) | Prostático (agrupado) | p < 0,001 ambos | [6] |
Tabla 1. Resumen de evidencia clave sobre reducción de densidad microvascular (DMV) y expresión de VEGF inducida por 5-ARI en tejido prostático humano. DM = diferencia de medias.
[18b] Donohue JF, et al. Randomized, placebo controlled trial showing that finasteride reduces prostatic vascularity rapidly within 2 weeks. BJU Int. 2005;96(9):1319–1322.
6. Un modelo bidireccional: involución tisular y regresión vascular
La relación entre la involución del tejido prostático y la regresión vascular es bidireccional. Por un lado, la reducción de DHT conduce a apoptosis epitelial y estromal, lo que disminuye la demanda metabólica y la señalización paracrina que sostienen el lecho microvascular [20][24]. Por otro lado, la regresión microvascular reduce el soporte trófico disponible para el tejido glandular, acelerando aún más la involución [19].
Este bucle de retroalimentación positiva explica por qué los efectos antiangiogénicos de los 5-ARI son detectables antes de que ocurra una reducción volumétrica significativa: la apoptosis de células endoteliales es un proceso relativamente rápido (días a semanas), mientras que la involución glandular requiere supresión androgénica sostenida durante meses [18b][25]. La implicación clínica es que incluso cursos preoperatorios cortos de 5-ARI (tan solo 2 semanas) pueden conferir beneficio hemostático durante la cirugía, como confirman los datos del metaanálisis [6].
Cabe destacar que la inhibición de la 5-alfa reductasa reduce el tamaño prostático en un 20–30% mediante la inducción de apoptosis, manifestada histológicamente como atrofia ductal, y disminuye el número de vasos sanguíneos a través de la reducción de VEGF [25]. Esta doble acción — volumétrica y vascular — distingue a los 5-ARI de los alfa-bloqueantes puros, que proporcionan alivio sintomático sin alterar la biología tisular subyacente.
7. Aplicación en hematospermia: extensión del fundamento antiangiogénico
Una aplicación clínica adicional que refleja directamente las propiedades antiangiogénicas de los 5-ARI es el tratamiento de la hematospermia (hemospermia). Aunque la hematospermia es habitualmente un proceso benigno y autolimitado, los casos persistentes o recurrentes pueden causar angustia significativa al paciente y representar un reto diagnóstico [27]. Las vesículas seminales y la uretra prostática comparten el mismo microambiente vascular dependiente de andrógenos que la zona de transición; en consecuencia, los mecanismos de reducción de DMV y supresión de VEGF descritos anteriormente son igualmente relevantes para este escenario clínico.
Badawy et al. (2012) realizaron un estudio prospectivo controlado con placebo evaluando finasterida 5 mg diarios durante 3 meses en 24 pacientes con hematospermia refractaria idiopática. En el grupo de finasterida, el 66,7% de los pacientes experimentaron remisión completa de los episodios de sangrado en 2–5 semanas, confirmado objetivamente mediante análisis de semen. En contraste, solo el 25% de los pacientes tratados con placebo mostraron mejoría, y aquellos que mejoraron aún demostraban eritrocitos residuales significativos en la microscopía (>50 GR/CGA). No se observó recurrencia durante el período de tratamiento de 3 meses en los respondedores [28].
Esta respuesta rápida — en semanas, no en meses — refleja la cronología de la reducción de DMV observada en los estudios preoperatorios de RTUp, reforzando el concepto de que el efecto antiangiogénico de los 5-ARI precede a la involución glandular y opera como el mecanismo primario de control del sangrado.
Zhang et al. (2014) reportaron la combinación de vesiculoscopia seminal transuretral (VSTU) con finasterida perioperatoria (5 mg/d durante 2 semanas pre y postoperatorias) en 32 pacientes con hematospermia recurrente. El abordaje combinado permitió tanto la evaluación diagnóstica como el tratamiento, con la finasterida proporcionando una reducción farmacológica de la vascularización tisular que complementó la intervención endoscópica [29].
En los algoritmos de manejo de la hematospermia, los 5-ARI están posicionados actualmente como una opción farmacológica para casos persistentes tras la exclusión de infección y malignidad, particularmente cuando la fuente de sangrado es de origen prostático o de las vesículas seminales [30][31]. El fundamento es mecánicamente idéntico al uso perioperatorio en RTUp: al reducir la expresión de VEGF y la DMV mediada por DHT en la vasculatura prostática y periprostática, la finasterida disminuye la fragilidad y densidad de los vasos submucosos propensos a la ruptura durante la erección y la eyaculación.
Existe una paradoja notable: la finasterida también ha sido reportada como causa rara de hematospermia, particularmente en hombres jóvenes que toman finasterida a dosis bajas (1 mg) para alopecia androgenética [32]. Esta aparente contradicción puede reflejar el remodelado vascular transitorio que ocurre durante la fase inicial del tratamiento, antes de que se establezca un nuevo estado estable de vascularización reducida. La significación clínica de este efecto paradójico parece ser mínima y autolimitada.
8. Implicaciones clínicas y quirúrgicas
Optimización preoperatoria para RTUp: El metaanálisis de Hehir et al. (2026) proporciona evidencia robusta de que la administración preoperatoria de 5-ARI reduce la pérdida sanguínea intraoperatoria, los requerimientos transfusionales, el volumen de irrigación y el tiempo operatorio durante la RTUp. Incluso cursos cortos de 2 semanas parecen ser efectivos, convirtiendo esto en una intervención preoperatoria práctica [6].
Manejo de la hematuria relacionada con HBP: Kearney et al. demostraron que la finasterida controla eficazmente la hematuria macroscópica secundaria a HBP, con un 94% de los pacientes experimentando mejoría y un 77% logrando resolución completa, independientemente del estado de anticoagulación [26]. Este efecto está mediado por la reducción de la DMV en el tejido prostático suburetral.
Potencial relevancia para procedimientos de enucleación: Aunque la evidencia actual se basa fundamentalmente en la RTUp, los mecanismos antiangiogénicos de los 5-ARI deberían teóricamente beneficiar cualquier procedimiento que implique disección transuretral de tejido prostático. Durante la enucleación con láser de holmio (HoLEP) y otras técnicas de enucleación, el sangrado del plano capsular es una consideración intraoperatoria significativa. Si la terapia preoperatoria con 5-ARI confiere ventajas hemostáticas similares durante la enucleación como lo hace durante la resección sigue siendo un área importante para investigación futura.
Pacientes anticoagulados: Los 5-ARI pueden ser particularmente valiosos en pacientes que requieren terapia anticoagulante o antiagregante continua y están en mayor riesgo de sangrado perioperatorio. La reducción de la vascularización tisular puede compensar parcialmente el deterioro hemostático sistémico en estos pacientes.
Figura 1. Modelo integrado de regresión vascular prostática inducida por 5-ARI
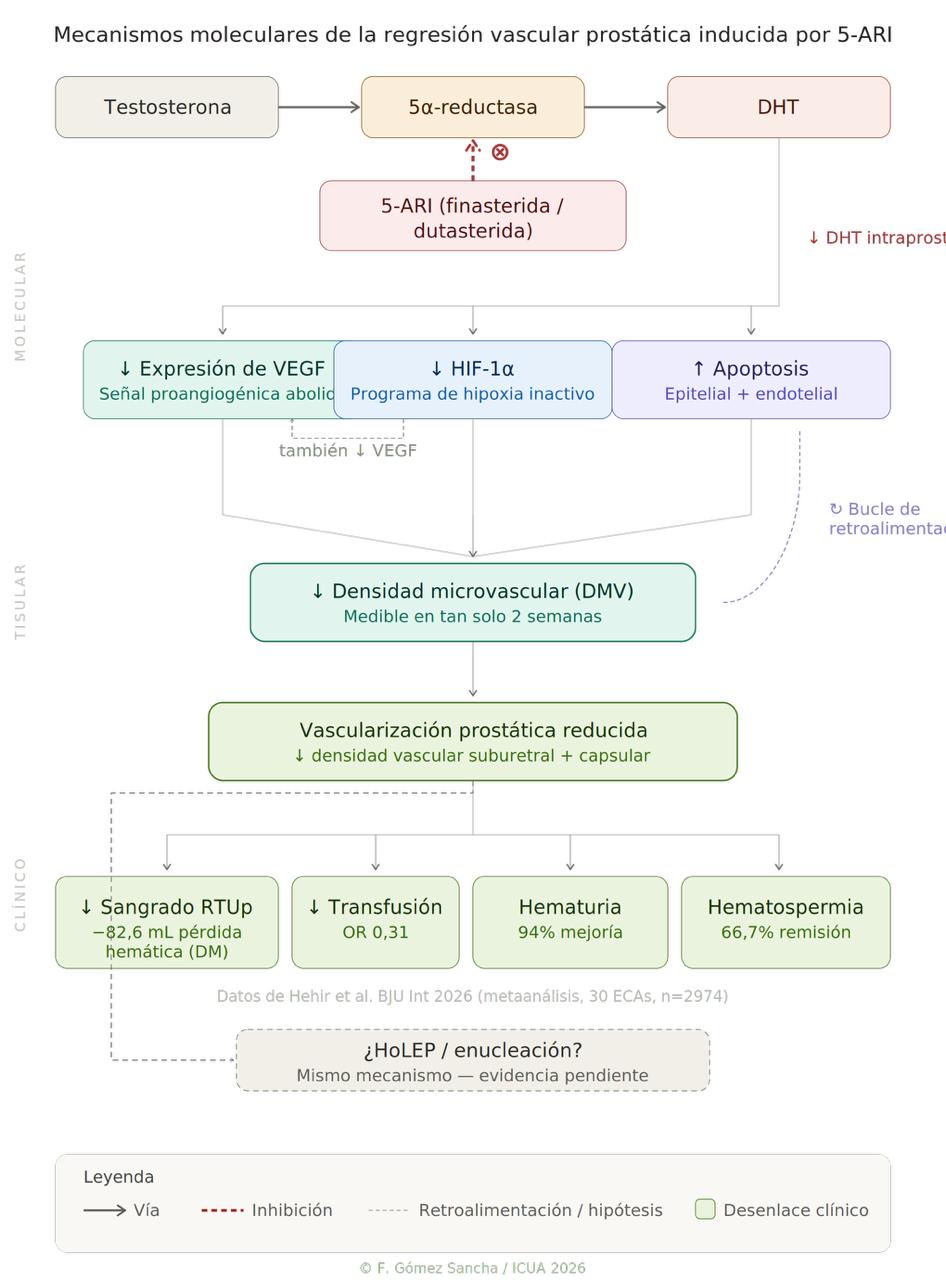
Figura 1. Modelo a tres niveles de la desvascularización prostática inducida por 5-ARI: vías moleculares, efectos tisulares y resultados clínicos.
9. Conclusión
Los inhibidores de la 5-alfa reductasa reducen la vascularización prostática a través de una cascada de mecanismos interconectados: supresión de la expresión de VEGF mediada por DHT, reducción de la densidad microvascular, inducción de apoptosis endotelial y epitelial, y modulación del programa angiogénico más amplio mediado por HIF-1α. Estos efectos ocurren rápidamente, con reducción medible de la DMV en 2 semanas de tratamiento, y están respaldados por evidencia de nivel 1 de ensayos clínicos aleatorizados agrupados.
Comprender estos mecanismos es importante no solo para optimizar el manejo perioperatorio en la cirugía de HBP, sino también para informar la toma de decisiones clínicas respecto al momento y duración de la terapia preoperatoria con 5-ARI. La investigación futura debería evaluar si estos beneficios antiangiogénicos se extienden a las técnicas modernas de enucleación, y si subgrupos específicos de pacientes (p. ej., aquellos bajo anticoagulación o con próstatas altamente vascularizadas) obtienen un beneficio desproporcionado de la administración preoperatoria de 5-ARI.
Referencias
[1] Roehrborn CG. Pathology of benign prostatic hyperplasia. Int J Impot Res. 2008;20 Suppl 3:S11–S18. PubMed
[2] Rittmaster RS. 5alpha-reductase inhibitors in benign prostatic hyperplasia and prostate cancer risk reduction. Best Pract Res Clin Endocrinol Metab. 2008;22(2):389–402. PubMed
[3] Traish AM, Mulgaonkar A, Giordano N. The dark side of 5α-reductase inhibitors' therapy. Korean J Urol. 2014;55(6):367–379. PubMed
[4] McConnell JD, et al. The long-term effect of doxazosin, finasteride, and combination therapy on clinical progression of BPH. N Engl J Med. 2003;349(25):2387–2398. PubMed
[5] Roehrborn CG, et al. Efficacy and safety of dutasteride in men with BPH. Urology. 2002;60(3):434–441. PubMed
[6] Hehir CM, et al. The role of 5-alpha reductase inhibitors in TURP: a meta-analysis of RCTs. BJU Int. 2026. doi: 10.1111/bju.70117. PubMed
[7] Chislett B, et al. 5-ARI use in prostatic disease and beyond. Transl Androl Urol. 2023;12(3):487–505. PMC
[8] Jackson MW, et al. VEGF expression in prostate cancer and BPH. J Urol. 1997;157(6):2323–2328. PubMed
[9] Ferrara N. Role of VEGF in the regulation of angiogenesis. Kidney Int. 1999;56(3):794–814. PubMed
[10] Bruchovsky N, Wilson JD. The conversion of testosterone to 5α-DHT by rat prostate. J Biol Chem. 1968;243(8):2012–2021. PubMed
[11] Carson C, Rittmaster R. The role of DHT in BPH. Urology. 2003;61(4 Suppl 1):2–7. PubMed
[12] Clark RV, et al. Marked suppression of DHT by dutasteride. J Clin Endocrinol Metab. 2004;89(5):2179–2184. PubMed
[13] Bramson HN, et al. Unique preclinical characteristics of GG745, a potent dual inhibitor of 5AR. J Pharmacol Exp Ther. 1997;282(3):1496–1502. PubMed
[14] Pareek G, et al. Effect of finasteride on VEGF expression and microvessel density. J Urol. 2003;169(1):20–23. PubMed
[15] Häggström S, et al. Testosterone induces VEGF synthesis in the ventral prostate in castrated rats. J Urol. 1999;161(5):1620–1625. PubMed
[16] Hochberg DA, et al. Decreased suburethral prostatic MVD in finasteride treated prostates. J Urol. 2002;167(4):1731–1733. PubMed
[17] Memis A, et al. Effect of finasteride on suburethral prostatic MVD. Urol Int. 2008;80(2):177–180. PubMed
[18] Donohue JF, et al. TURP and bleeding: RCT of finasteride for decreasing blood loss. J Urol. 2002;168(5):2024–2026. PubMed
[18b] Donohue JF, et al. Finasteride reduces prostatic vascularity rapidly within 2 weeks. BJU Int. 2005;96(9):1319–1322. PubMed
[19] Sutton M, et al. Finasteride targets prostate vascularity by inducing apoptosis and inhibiting cell adhesion. Prostate. 2006;66(11):1194–1202. PubMed
[20] Rittmaster RS, et al. Evidence for atrophy and apoptosis in the rat prostate with finasteride. Endocrinology. 1995;136(2):741–748. PubMed
[21] Lekas AG, et al. Finasteride effects on hypoxia and angiogenetic markers in BPH. Urology. 2006;68(2):436–441. PubMed
[22] Semenza GL. Targeting HIF-1 for cancer therapy. Nat Rev Cancer. 2003;3(10):721–732. PubMed
[23] Ku JH, et al. Effect of dutasteride on HIF-1α, VEGF and MVD in rat and human prostate tissue. Scand J Urol Nephrol. 2009;43(6):445–453. PubMed
[24] Tian HL, et al. Finasteride reduces MVD and VEGF in renal tissue of diabetic rats. Am J Med Sci. 2015;349(6):516–520. PubMed
[25] Naslund MJ, Miner M. Clinical efficacy and safety of 5-ARIs for the enlarged prostate. Clin Ther. 2007;29(1):17–31. PubMed
[26] Kearney MC, et al. Finasteride for control of gross hematuria due to BPH. J Urol. 2002;167(6):2489–2491. PubMed
[27] Ahmad I, Krishna NS. Hemospermia. J Urol. 2007;177(5):1613–1618. PubMed
[28] Badawy AA, et al. Finasteride for treatment of refractory hemospermia: prospective placebo-controlled study. Int Urol Nephrol. 2012;44(2):371–375. PubMed
[29] Zhang K, et al. Transurethral seminal vesiculoscopy combined with finasteride for recurrent hematospermia. Zhonghua Nan Ke Xue. 2014;20(5):449–452. PubMed
[30] Efesoy O, et al. Novel algorithm for the management of hematospermia. Urol Res Pract. 2023;49(6):398–405.
[31] Mathers MJ, et al. Hematospermia: etiology, diagnosis, and treatment. Dtsch Arztebl Int. 2017;114(45):757–762. PubMed
[32] Alharbi FF, et al. Hematuria and hematospermia associated with finasteride for androgenic alopecia. Drug Saf Case Rep. 2017;4(1):14. PubMed





No hay comentarios:
Publicar un comentario